近日,中国科学院北京生命科学研究院高福课题组联合上海巴斯德所周东明课题组在寨卡病毒疫苗研究上取得重要进展。研究成果以题为“Recombinant Chimpanzee Adenovirus Vaccine AdC7-M/E Protects against Zika Virus Infection and Testis Damage”(重组黑猩猩腺病毒疫苗AdC7-M/E抵御寨卡病毒感染及其造成的睾丸损伤)1月3日在线发表在Journal of Virology上。
寨卡病毒属于黄病毒科黄病毒属,是一种主要由蚊虫传播的病原。2015年巴西暴发寨卡疫情并迅速在南美和中北美蔓延,进一步扩散到全球80多个国家和地区。2016年2月我国报道首例输入性寨卡病例,至今已有数十例。寨卡感染能够引起许多神经系统疾病,如格林巴利综合征,最为严重的是会导致胎儿发育缺陷形成新生儿的小头畸形。另外,寨卡病毒可以通过性传播而突破血脑、血胎、血睾和血眼这人体四大屏障。2016年2月至11月期间世界卫生组织宣布寨卡病毒及其引起的新生儿小头症疫情为国际公共卫生紧急事件。目前,该疾病尚无获批疫苗和有效治疗手段,对社会公共卫生安全构成了严重威胁。因此寨卡疫苗的研制显得非常迫切。
科研团队选择黑猩猩腺病毒开发疫苗的载体。重组腺病毒疫苗具有较强的免疫能力、维持周期长、免疫宿主广泛、不需要添加佐剂、易于工厂化生产等优点,7型黑猩猩腺病毒(AdC7)在中国人群中预存免疫仅为11.8%,远小于常用的5型人腺病毒(HuAd5)的74.2%,因此。研究利用分子生物学方法将寨卡病毒的M/E基因克隆到AdC7载体中,然后包装出有活性的表达寨卡病毒M/E蛋白的重组黑猩猩腺病毒载体疫苗AdC7-M/E(图1)。AdC7-M/E免疫小鼠后1周即可激活产生较高的中和抗体,并可较长时间的维持很高的中和抗体水平。该疫苗也可以同时激活很强的特异性T细胞反应。一针免疫可以完全保护免疫缺陷小鼠免受致死剂量的寨卡病毒的感染,并实现清除性免疫的效果,即血清和靶组织器官都够检测不到病毒RNA的存在。前期该团队在Cell杂志上报道了寨卡病毒感染免疫缺陷小鼠会出现睾丸组织损伤及萎缩, AdC7-M/E疫苗能够很好的保护睾丸免受损伤(图2)。以上研究结果表明AdC7-M/E是一个高效的抗寨卡病毒疫苗,将具有很大的临床应用前景。
中科院北京生命科学研究院博士生徐坤和中科院上海巴斯德研究所副研究员宋宇峰为共同第一作者。中科院北京生命科学研究院、微生物所、中国疾控中心高福研究员和中科院上海巴斯德研究所周东明研究员为论文共同通讯作者。该项目得到了中科院先导培育项目(XDPB0301)、国家重点研发计划项目(2016YFC1201000和2016YFE0205800)、国际科技重大专项项目(2016ZX10004222-008)、中科院国际合作项目(153211KYSB20160001)和国家自然基金创新群体项目(81621091)的支持。
此外,该团队去年已开发了一种预防寨卡感染的灭活疫苗,并转让给长春长生生物科技有限责任公司进行后续开发(http://www.im.cas.cn/xwzx/jqyw/201705/t20170527_4805236.html)。
全文链接
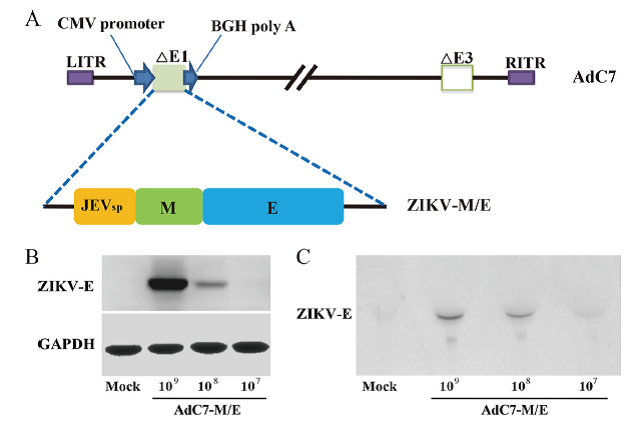
AdC7-M/E疫苗的构建与抗原表达
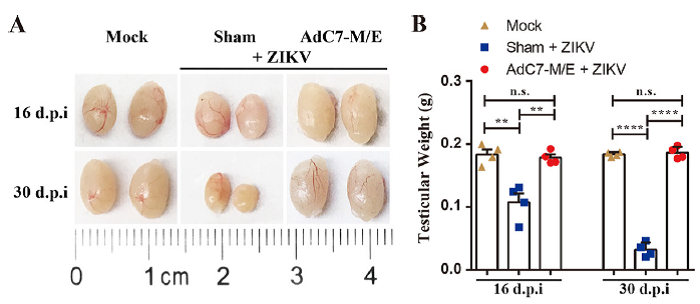
AdC7-M/E疫苗保护睾丸免受寨卡病毒引起的损伤和萎缩

